

雷晓光课题组与合作者发现诱导细胞免疫反应的新型天然产物佐剂分子

佐剂是疫苗的关键成分,可增强抗原特异性免疫反应。然而,新型疫苗佐剂开发一直是预防医疗创新最慢的方面之一。迄今为止,只有少数佐剂获得批准用于人类疫苗。1926年发现的第一种佐剂铝佐剂是许可产品中应用最广泛的佐剂。其功效归因于诱导辅助T细胞2(TH2)反应,产生高水平抗体。但铝佐剂很少或不刺激辅助T细胞1(TH1)或细胞毒性T淋巴细胞(CTL)免疫反应,使其不足以触发对抵抗细胞内病原体和肿瘤至关重要的细胞免疫应答。因此,临床上迫切需要能够有效增强细胞免疫的新型佐剂。
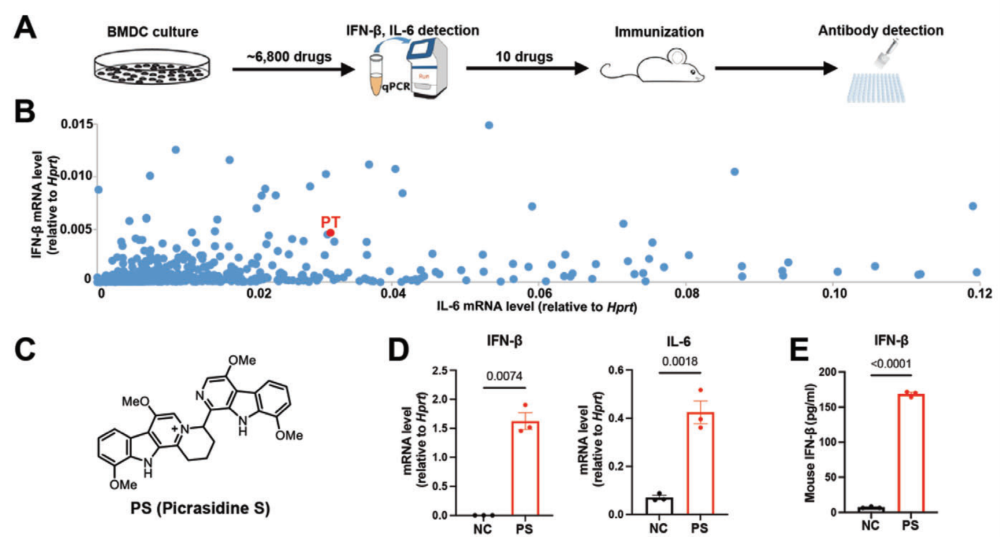
受近期发现的I型干扰素(IFN-I)信号增强T细胞免疫反应的启发,该研究提出,靶向该途径可能成为鉴定新型疫苗佐剂的有效策略。通过对6,800个小分子全面筛选,作者发现天然产物Picrasidine S(PS)有效诱导IFN-β。雷晓光课题组前期利用C-H键官能团化策略完成了该类天然产物生物碱的高效、集体全合成,为后期的生物学研究提供了物质基础(Qixuan Wang, Fusheng Guo, Jin Wang, Xiaoguang Lei* “Divergent Total Syntheses of ITHQ-type Bis-β-carboline Alkaloids by Regio-selective Formal Aza-[4+2] Cycloaddition and Late-stage C-H Functionalization” Chem. Sci. 2023, 14, 10353-10359)。为了评估其作为佐剂的效果,研究人员在不同类型抗原免疫及肿瘤模型中做了检测,并与应用最广泛的佐剂铝佐剂做了对比。结果表明,PS作为佐剂能有效增强体液免疫和细胞免疫反应,并且无明显毒副作用。
为了确定PS在体内发挥免疫调节功能是否依赖于IFN-I,作者分别用anti-IFNAR-1抗体和IFNα/β受体敲除(IFNα/βR−/−)小鼠做了验证,共同证实IFN-I在PS诱导的免疫反应中有重要功能。进一步研究发现,PS在表达cGAS的细胞中强烈触发IFN-β,而在cGAS敲除细胞中IFN-β显著减少。结合cGAS基因敲除(cGAS−/−)小鼠,作者证实PS通过cGAS-IFN-I信号通路增强T细胞免疫反应,特别是通过增加CD8+中央记忆(TCM)样细胞介导抗肿瘤免疫应答增强。
综上所述,该研究阐明了天然产物PS作为疫苗佐剂的重要功能及作用机制,为新型疫苗佐剂开发和癌症预防提供了新的候选分子和理论依据。
北京分子科学国家研究中心雷晓光教授和清华大学基础医学院免疫所曾文文教授为该论文的共同通讯作者。清华大学基础医学院博士后丁晓凡、博士生孙梦雪、北京大学化学与分子工程学院博士后郭富生、清华大学基础医学院已毕业博士生钱鑫民为共同第一作者。该研究得到了国家自然科学基金、国家重点研发计划、北京市自然科学基金、中国博士后科学基金、北京分子科学国家研究中心、北大-清华生命科学联合研究中心、清华大学免疫学研究所、基础医学院等项目和单位的支持。