

李峻柏课题组在仿生超分子组装方面取得新进展
在国家自然科学基金委、科技部及中国科学院的支持下,北京分子科学国家研究中心李峻柏课题组多年来在模拟线粒体的结构与功能方面进行了深入研究,取得了系列进展。通过整合自然ATP合成酶与人工酶(纳米金,Angew. Chem. Int. Ed., 2019, 58, 5572-5576;聚天青,CCS Chem., 2023, 5, 1644-1652;氮化碳,J. Am. Chem. Soc.,2023, 145, 20907-20912),有效模拟了自然线粒体的能量合成功能。他们还利用Au-S单层自组装技术 (Angew. Chem. Int. Ed., 2019, 58, 1110-1114)及硼酸酯化学(Angew. Chem. Int. Ed., 2021, 60,7695-7698)等非生物化学过程,为仿生系统中生物能量转换提供驱动力,展现了非生物化学过程调控生物能量转换的潜力。
最近,该课题组利用溶胶-凝胶技术制备了可高负载还原性辅酶I(NADH)的树枝状介孔二氧化硅微粒(DMSM),在其表面铺展同时含ATP合成酶和人工电子穿梭体的蛋白脂质体,构建了一种仿线粒体微反应器。研究表明,电子穿梭体可介导膜内外的电子传递,引发NADH的氧化反应生成氧化性辅酶I(NAD+)和质子,形成的跨膜质子梯度势驱动ATP合成酶合成ATP 。DMSM的多级结构与孔隙特性提高了NADH装载量,促进了传质并稳定了蛋白脂质体,最终实现了生物能量合成的有效增强。该工作为深入理解生物体内能量代谢过程提供了新视角,也为人工提升生物能量合成代谢提供了新思路。
相关成果近期发表于Angew. Chem. Int. Ed., 2024, 63, e202319116,论文第一作者为博士研究生王彤晖,通讯作者为李峻柏研究员和费进波研究员。
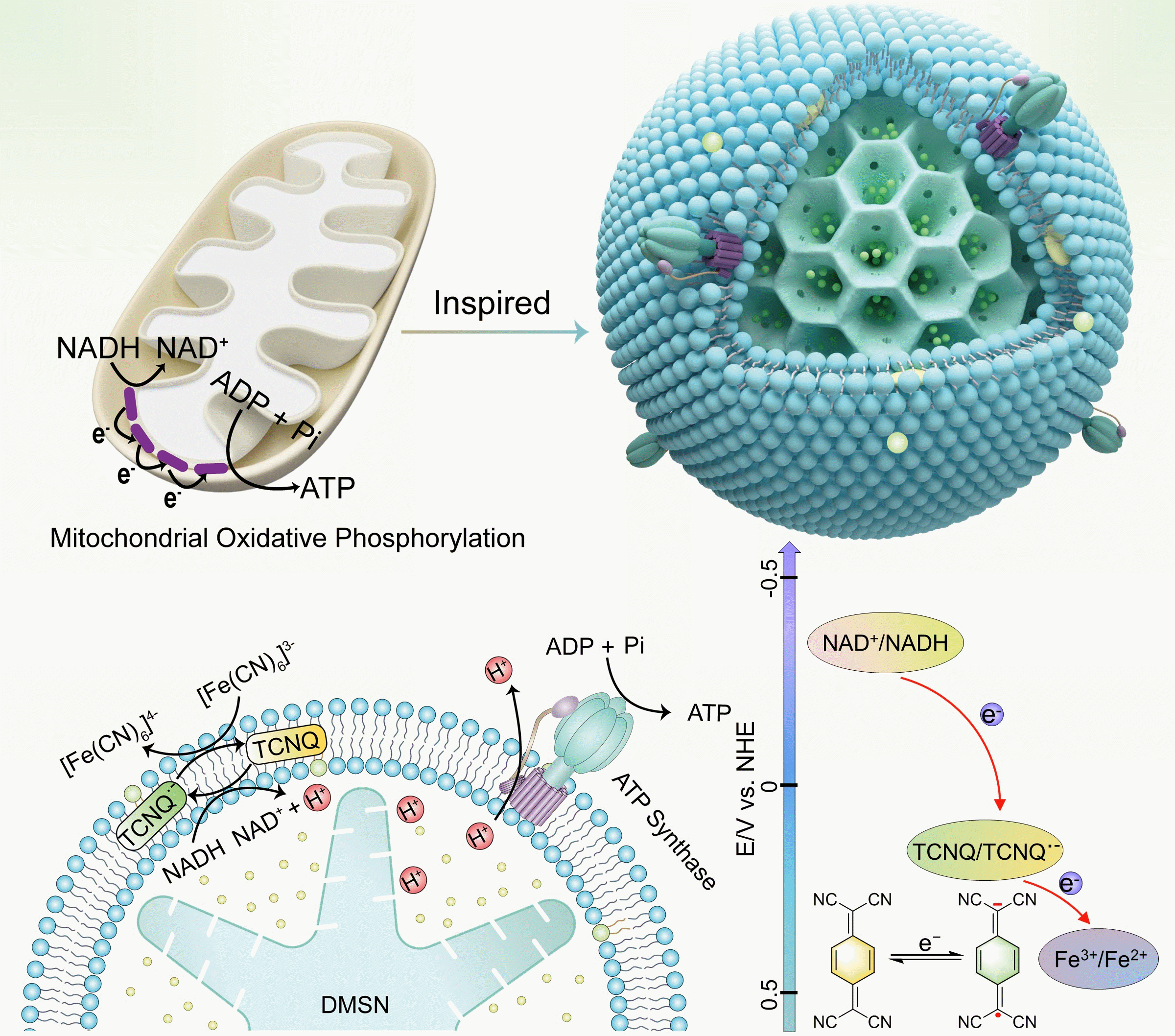
仿线粒体增强生物能量合成