

赵睿课题组在靶向多肽调控膜蛋白细胞间聚集方面取得新进展
细胞通讯精密控制生命系统的稳态平衡,在细胞生长、发育、分化和死亡等生命活动中发挥重要作用。跨膜蛋白参与细胞内外、细胞之间的物质和信号交换,是认识和调节这一重要生理过程的关键靶标。然而,如何针对膜蛋白灵活多变以及难以稳定结合的结构,设计高特异性亲和分子探针并开展靶向探测和化学干预,极具挑战和重要科学意义。
在国家自然科学基金委和中国科学院的支持下,北京分子科学国家研究中心赵睿课题组长期致力于正-反义肽相互作用原理及其规律的研究。针对细胞通讯关键四次跨膜蛋白CD81,提出利用遗传密码子简并性构建亲和力可编辑多肽的策略。发展了具有单残基分辨能力的均相亲和筛选新体系,成功获得了位点特异性识别并稳定结合CD81蛋白胞外小环的多肽,其结合自由能为-9.56 kcal/mol。利用新型反义肽为分子探针,发现并解析了CD81蛋白在单个乳腺癌细胞和细胞接触界面的分布差异。进一步研究显示,亲和多肽与CD81蛋白胞外小环的特异性识别结合是触发蛋白向细胞紧密连接重新定位和靶向聚集的关键信号,揭示了之前少有研究的胞外小环在介导细胞-细胞相互作用中的关键作用。基于亲和多肽在CD81蛋白功能调控中的潜能,建立了多肽介导的肿瘤细胞迁移的靶向干预新方法,实现了CD81蛋白表达响应的肿瘤细胞迁移抑制。将多肽用于活体抗肿瘤生长与转移抑制分析,在小鼠模型中实现了高侵袭性三阴性乳腺癌肺转移的高效靶向抑制,为恶性肿瘤的精准诊疗提供了新靶标和新工具。相关研究工作发表在Angew. Chem. Int. Ed.期刊(https://doi.org/10.1002/anie.202400129),文章第一作者为博士生徐坤,通讯作者为赵睿研究员和黄嫣嫣研究员。
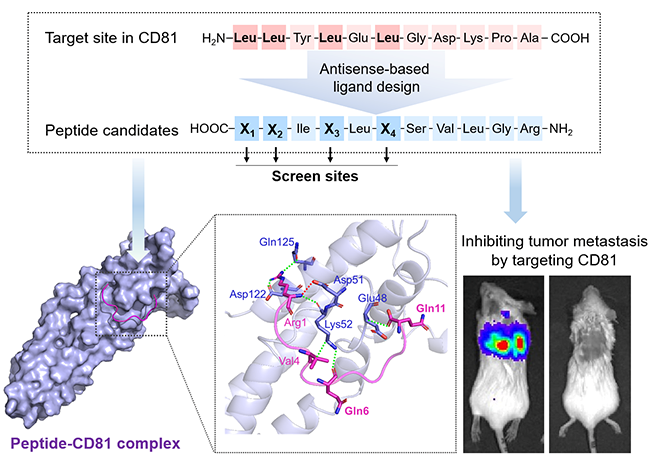
跨膜蛋白靶向多肽的设计、位点特异性结合及恶性肿瘤转移抑制