

化学生物学研究部张文彬课题组在拓扑蛋白质的合成和表征方面取得重要进展
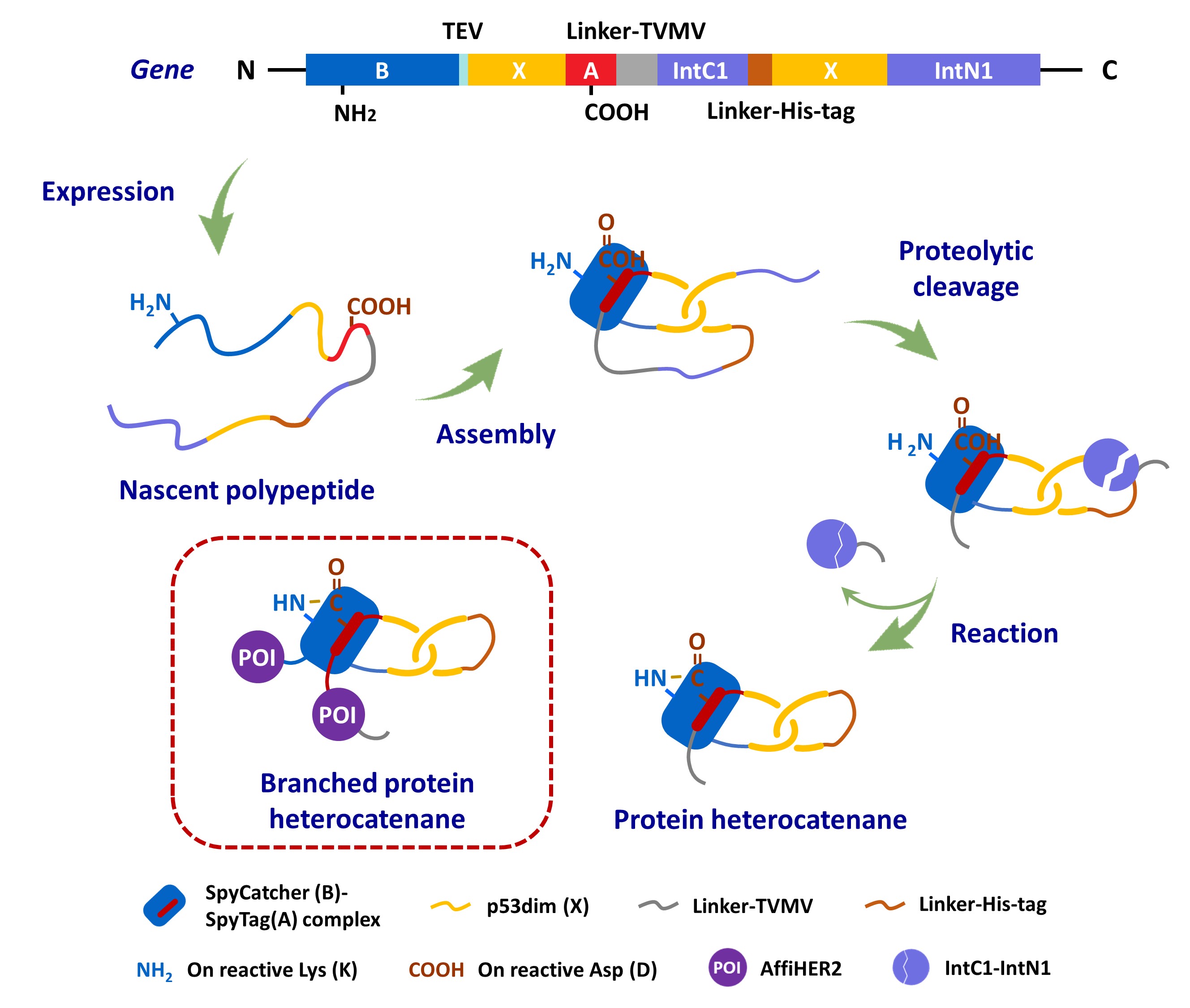
图1. 通过原位酶切、谍标签-谍捕手反应对和分离型内含肽共同介导(支化)蛋白质异质索烃的生物合成
为进一步简化合成过程,他们基于分离型内含肽在反应时会自身从主链上切除下来的特性,设计了由两种正交的分离型内含肽介导的环化过程,其可以在胞内次序发生反式剪接和自发链断裂,从而消除了原位酶切反应的必要性,并可实现两个蛋白质结构域的主链环化,制备结构更加简洁的蛋白质异质索烃(图2)。X射线单晶衍射实验成功解析了利用该方法制备的cat-GFPX-X的晶体结构,有力地证明了其中两个环状组分之间机械互锁的空间关系(图3)。这也是第一个人工设计合成的蛋白质异质索烃的晶体结构。
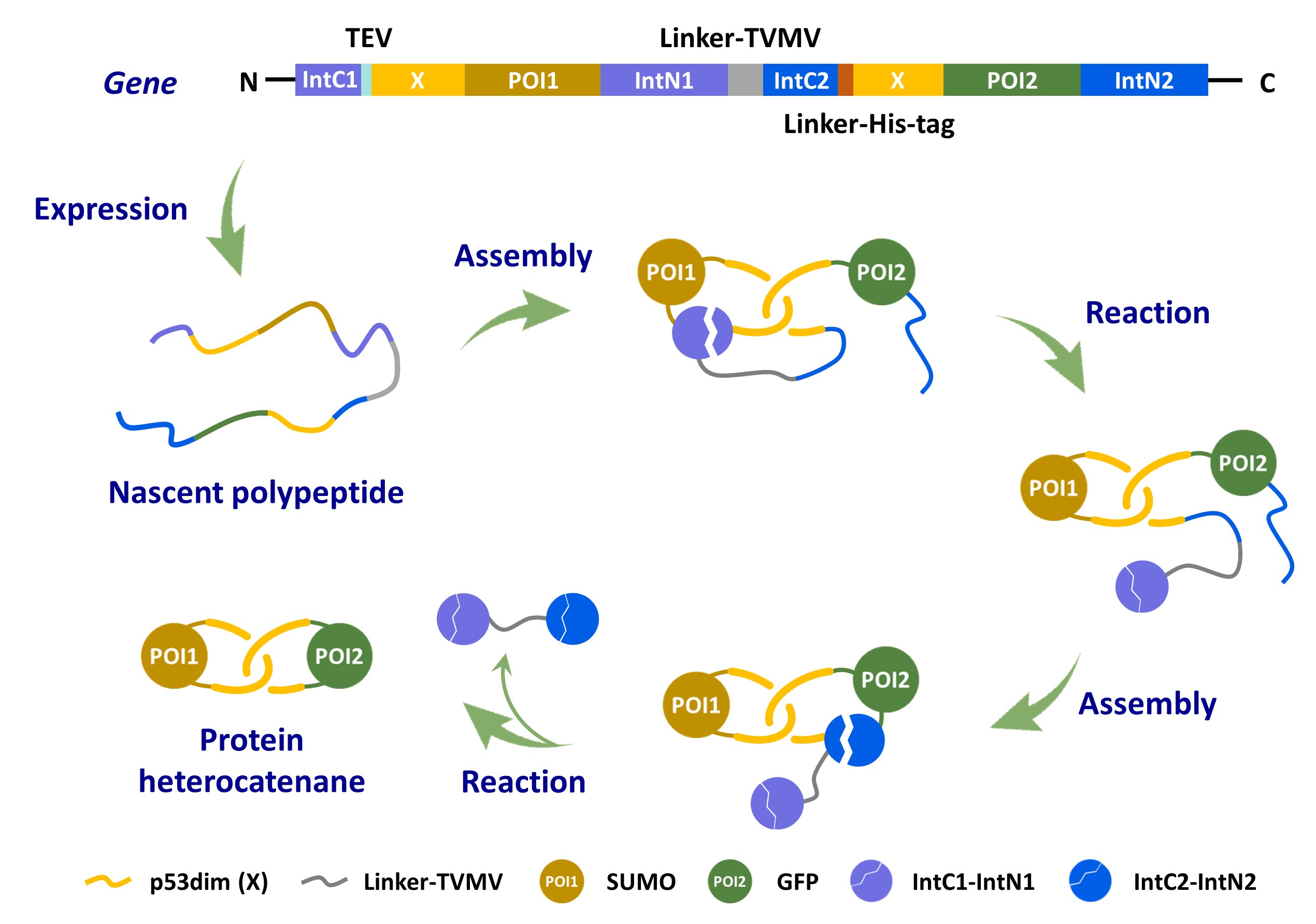
图2. 由两种正交的分离型内含肽介导蛋白质异质索烃的生物合成
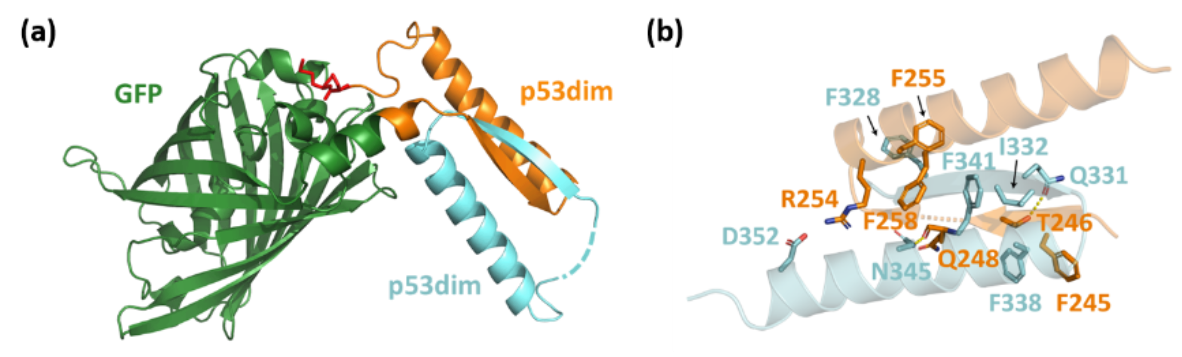
图3. (a)利用X射线衍射解析所得cat-GFPX-X晶体结构(PDB ID: 7BWN);(b) cat-GFPX-X晶体结构中两个p53dim结构域的相互作用界面分析
该方法的优势在于其可基因编码,高度模块化,且合成过程无需额外控制,在细胞内直接自发完成,既大大简化了合成步骤,又有效提高了产物的纯度。它适用于胞内合成含有多种功能蛋白质的异质索烃,并可拓展到各种具有支化结构的异质索烃。相较于同质索烃,它们的分子结构复杂性和多样性进一步提高,有望更好地实现不同结构域之间的协同,深入地探讨拓扑结构对分子性质和功能的影响,在工业酶工程和生物医药领域具有广泛的潜在应用价值。该研究近期在线发表于Angew. Chem. Int. Ed.。
原文链接:https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.202005490